Il pimecrolimus nel trattamento dell'eczema: nessun rischio cancerogeno?
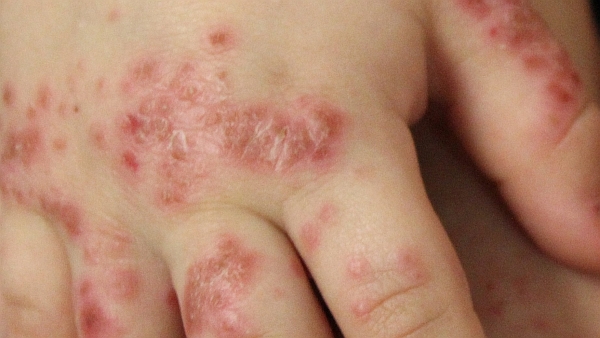
Secondo uno studio recentemente pubblicato su JAMA Dermatology, la terapia a base di pimecrolimus topico per l'eczema potrebbe non comportare rischi cancerogeni, contrariamente a quanto affermato nell'informativa redatta dall'FDA.
"In questo momento, i dati clinici non sembrano supportare i dubbi circa la sicurezza di impiego del pimecrolimus", ha dichiarato l'autore dello studio, il Dr. David Margolis, professore di Dermatologia presso la University of Pennsylvania di Philadelphia.
"Quando il pimecrolimus è stato presentato per la prima volta, faceva parte di una nuova classe di farmaci per uso topico. I dubbi circa la sua sicurezza non nascevano dalla valutazione dei dati clinici raccolti durante la fase sperimentale, ma piuttosto dai potenziali effetti della molecola stessa", ha continuato il Dr. Margolis.
Il pimecrolimus, un inibitore della calcineurina, è una delle poche sostanze per uso topico che ha ricevuto l'approvazione per l'impiego nella terapia dell'eczema nei bambini, ma l'FDA ha rilasciato un'informativa nella quale si evidenziava il suo potenziale cancerogeno. L'allarme deriva da dati raccolti circa l'impiego orale e topico in studi su animali e da studi di casi su pazienti umani. Per questo motivo, l'FDA annovera questa sostanza fra le terapie di seconda linea.
Il Dr. Margolis e colleghi hanno condotto un'analisi sui dati raccolti nell'arco di dieci anni da quasi 7500 pazienti pediatrici coinvolti in uno studio a lungo termine sull'eczema infantile (PEER).
In quasi 27.000 persone-anno, i pazienti hanno sviluppato cinque neoplasie maligne, nessuna delle quali era un tumore cutaneo. La percentuale standardizzata di incidenza non è quindi statisticamente differente da quella calcolata a partire dal database della popolazione generale del National Cancer Institute.
"Alla luce di questi dati, l'allarme lanciato dall'FDA potrebbe aver allontanato i pazienti da un trattamento dal quale avrebbero potuto trarre reali benefici", ha commentato il Dr. Jon Hanifin, dermatologo presso la Oregon Health and Science University di Portland.
"La dermatite atopica è una malattia che provoca disagio, ansia e insonnia nei pazienti, ma questo genere di problemi sembra essere ignorato da molti medici ed anche dall'FDA. Questi pazienti hanno bisogno di aiuto ma l'FDA ed i suoi consulenti medici sembrano aver deciso di gestire la situazione con grande lentezza", ha proseguito il Dr. Hanifin.
"Questo nuovo studio potrebbe migliorare significative le prospettive di trattamento per questi pazienti.
Alcune associazioni di categoria, fra le quali la American Academy of Dermatology e la National Eczema Association, stanno premendo perché l'FDA accelleri il processo di approvazione di nuovi farmaci per il trattamento dell'eczema nei bambini.
La Valeant Pharmaceuticals International, azienda produttrice di Elidel, nome commerciale del pimecrolimus per uso topic, ha finanziato lo studio tramite sovvenzioni alla University of Pennsylvania.
Riferimenti:
JAMA Dermatology, February 18, 2015